sábado, 1 de septiembre de 2018
semana 28
Durante esta semana se realiza la decoración para la celebración del día de la antioqueñidad
Semana 27
Mecanismos de sustitución no polar
Mecanismo de la reacción
Las halogenaciones radicalarias trancurren en tres etapas denominadas: iniciación, propagación y terminación:
Etapa de iniciación
En el primer paso de la reacción se produce la rotura homolítica del enlace Cl-Cl. Esto se consigue con calor o mediante la absorción de luz.
Primera etapa de propagación
Se trata de una etapa ligeramente endotérmica que consiste en la sustracción de un hidrógeno del metano por el radical cloro formado en la etapa anterior, generándose el radical metilo.
Segunda etapa de propagación
Durante la misma el radical metilo abstrae un átomo de cloro de una de las moléculas iniciales, dando clorometano y un nuevo átomo de cloro. Dicho átomo vuelve a la primera etapa de propagación y se repite todo el proceso.
Etapa de terminación
Tiene lugar cuando se agotan los reactivos, entonces los radicales que hay en el medio se unen entre si.
semana 26
Reacción químicas orgánicas
Las reacciones orgánicas son reacciones químicas que involucran al menos un compuesto orgánico como reactivo. Los tipos básicos de reacciones químicas orgánicas son reacciones de adición, reacciones de eliminación, reacciones de sustitución, y reacciones redox orgánicas.
En síntesis orgánica, se usan reacciones orgánicas en la construcción de nuevas moléculas orgánicas. La producción de muchos químicos hechos por el hombre, tales como drogas, plásticos, aditivos alimentarios, textiles, dependen de las reacciones orgánicas.
Reactivos orgánicos
Electrofilo
Un electrófilo es un reactivo químico atraído hacia zonas ricas en electrones que participa en una reacción química aceptando un par de electrones formando un enlace con un nucleófilo. Ya que los electrófilos aceptan electrones, ellos son ácidos de Lewis (ver teorías de reacciones ácido-base). La mayoría de los electrófilos están cargados positivamente, tienen un átomo que lleva una carga positiva parcial o bien no posee un octeto de electrones.
Nucleofilo
En química un nucleófilo es una especie que reacciona cediendo un par de electrones libres a otra especie (el electrófilo), combinándose y enlazándose covalentemente con ella. Un nucleófilo, concepto cinético, es también por definición una base de Lewis, concepto termodinámico. Un nucleófilo puede ser un anión o una molécula neutra con un par de electrones libres.
Las reacciones orgánicas son reacciones químicas que involucran al menos un compuesto orgánico como reactivo. Los tipos básicos de reacciones químicas orgánicas son reacciones de adición, reacciones de eliminación, reacciones de sustitución, y reacciones redox orgánicas.
En síntesis orgánica, se usan reacciones orgánicas en la construcción de nuevas moléculas orgánicas. La producción de muchos químicos hechos por el hombre, tales como drogas, plásticos, aditivos alimentarios, textiles, dependen de las reacciones orgánicas.
Reactivos orgánicos
Electrofilo
Un electrófilo es un reactivo químico atraído hacia zonas ricas en electrones que participa en una reacción química aceptando un par de electrones formando un enlace con un nucleófilo. Ya que los electrófilos aceptan electrones, ellos son ácidos de Lewis (ver teorías de reacciones ácido-base). La mayoría de los electrófilos están cargados positivamente, tienen un átomo que lleva una carga positiva parcial o bien no posee un octeto de electrones.
Nucleofilo
En química un nucleófilo es una especie que reacciona cediendo un par de electrones libres a otra especie (el electrófilo), combinándose y enlazándose covalentemente con ella. Un nucleófilo, concepto cinético, es también por definición una base de Lewis, concepto termodinámico. Un nucleófilo puede ser un anión o una molécula neutra con un par de electrones libres.
semana 25
Laboratorio ácidos carboxilicos
Clasificación de los azucares:

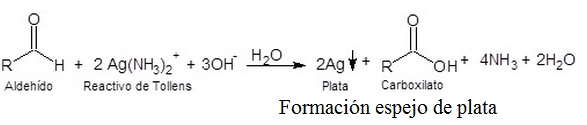
El reactivo de Tollens
El reactivo de Tollens es un complejo acuoso de diamina-plata, presentado usualmente bajo la forma de nitrato. Recibe ese nombre en reconocimiento al químico alemán Bernhard Tollens. Se usa en ensayos cualitativos de aldehidos, cetonas y enoles.
El reactivo de Baeyer
El reactivo de Baeyer es una solución alcalina de permanganato de potasio en solución básica, que es un potente oxidante. La reacción con los enlaces dobles (-C=C-) o triples (-C≡C-) en un material orgánico ocasiona que el color se desvanezca de púrpura-rosado a marrón. Los aldehídos y el ácido fórmico (y los ésteres de ácido fórmico) también dan una prueba positiva.
El reactivo de Biuret

El reactivo de Lucas
Clasificación de los azucares:

El reactivo de Tollens
El reactivo de Tollens es un complejo acuoso de diamina-plata, presentado usualmente bajo la forma de nitrato. Recibe ese nombre en reconocimiento al químico alemán Bernhard Tollens. Se usa en ensayos cualitativos de aldehidos, cetonas y enoles.
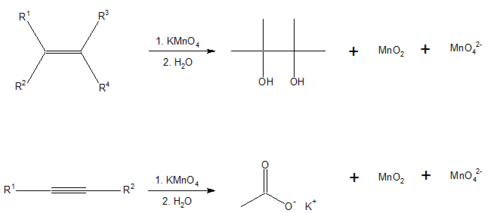
El reactivo de Baeyer
El reactivo de Baeyer es una solución alcalina de permanganato de potasio en solución básica, que es un potente oxidante. La reacción con los enlaces dobles (-C=C-) o triples (-C≡C-) en un material orgánico ocasiona que el color se desvanezca de púrpura-rosado a marrón. Los aldehídos y el ácido fórmico (y los ésteres de ácido fórmico) también dan una prueba positiva.

El reactivo de Biuret
Está hecho de hidróxido potásico (KOH) y sulfato cúprico (CuSO4), junto con tartrato de sodio y potasio (KNaC4O6·4H2O). El reactivo, cambia a violeta en presencia de proteínas, y vira a rosa cuando se combina con polipéptidos de cadena corta. El hidróxido de potasio no participa en la reacción, pero proporciona el medio alcalino necesario para que tenga lugar.
Se usa normalmente en el ensayo de Biuret, un método colorimétrico que permite determinar la concentración de proteínas de una muestra mediante espectroscopía ultravioleta-visible a una longitud de onda de 540 nm (para detectar el ion Cu2+).

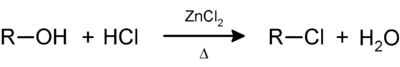
El reactivo de Lucas
El reactivo de Lucas es una solución de ZnCl2 disuelto en HCl concentrado que se usa en química orgánica. Esta disolución es usada para clasificar alcoholes de bajo peso molecular. La reacción es una sustitución en el cual el cloruro reemplaza el grupo hidroxilo. Un ensayo positivo es indicado por un cambio desde una solución limpia y sin color a una turbidez, que se trata de la formación de un cloroalcano.
semana 24
ISOMERÍA ÓPTICA
Existen moléculas que coinciden en todas sus propiedades excepto en su capacidad de desviar el plano de luz polarizada. Son los llamados isómeros ópticos. Uno de ellos desvía la luz hacia la derecha, y se designa (+), o dextrógiro, mientas que el otro la desvía en igual magnitud pero hacia la izquierda, y se designa (-) o levógiro. El aparato que aparece en la foto de la derecha es un polarímetro.
Para entender cómo funciona observa las animaciones de la Tabla inferior

Su comportamiento frente a la luz polarizada se debe a que la molécula carece de plano de simetría, y por lo tanto se pueden distinguir dos isómeros que son cada uno la imagen especular del otro, como la mano derecha lo es de la izquierda. Ambas manos no son iguales (el guante de una no encaja en la otra), pero son simétricas: la imagen especular de la mano derecha es la mano izquierda. Los isómeros ópticos también se llaman enantiómeros, enantiomorfos o isómeros quirales. El caso más frecuente de ausencia de plano de simetría se debe a que algún carbono tetraédrico está unido a cuatro radicales distintos (Figura de la derecha). Este carbono recibe el nombre de carbono asimétrico.
Existen moléculas que coinciden en todas sus propiedades excepto en su capacidad de desviar el plano de luz polarizada. Son los llamados isómeros ópticos. Uno de ellos desvía la luz hacia la derecha, y se designa (+), o dextrógiro, mientas que el otro la desvía en igual magnitud pero hacia la izquierda, y se designa (-) o levógiro. El aparato que aparece en la foto de la derecha es un polarímetro.
Para entender cómo funciona observa las animaciones de la Tabla inferior
Su comportamiento frente a la luz polarizada se debe a que la molécula carece de plano de simetría, y por lo tanto se pueden distinguir dos isómeros que son cada uno la imagen especular del otro, como la mano derecha lo es de la izquierda. Ambas manos no son iguales (el guante de una no encaja en la otra), pero son simétricas: la imagen especular de la mano derecha es la mano izquierda. Los isómeros ópticos también se llaman enantiómeros, enantiomorfos o isómeros quirales. El caso más frecuente de ausencia de plano de simetría se debe a que algún carbono tetraédrico está unido a cuatro radicales distintos (Figura de la derecha). Este carbono recibe el nombre de carbono asimétrico.
semana 23
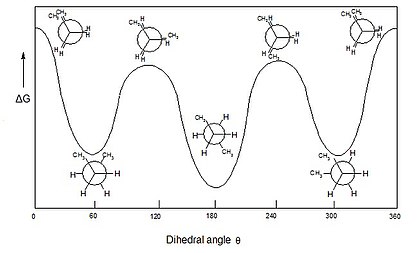
Isomería conformacional
En química orgánica, los isómeros conformacionales o confórmeros son estereoisómeros que se caracterizan por poder interconvertirse (modificar su orientación espacial, convirtiéndose en otro isómero de la misma molécula) a temperatura ambiente, por rotación en torno a enlaces simples. Estas conformaciones se denominan: anti, eclipsada o alternada. Son compuestos que, generalmente, no pueden aislarse físicamente, debido a su facilidad de interconversión.
El análisis conformacional es la exploración de todos los confórmeros que se pueden obtener de una molécula dada al realizar torsiones alrededor de enlaces sencillos (grados de libertad conformacionales), observando los cambios en la energía molecular asociados a esas torsiones.
semana 22
Isómeros estructurales
Definición de isómeros
Se llaman isómeros a moléculas que tienen la misma formula molecular pero distinta estructura. Se clasifican en isómeros de cadena, posición y función.
Isómeros de cadena
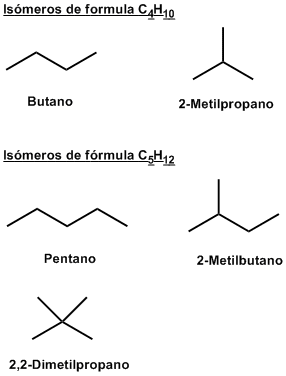
Se distinguen por la diferente estructura de las cadenas carbonadas. Un ejemplo de este tipo de isómeros son el butano y el 2-metilpropano.
Isómeros de posición
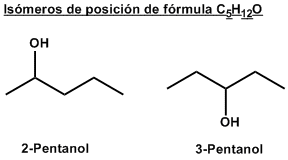
El grupo funcional ocupa una posición diferente en cada isómero. El 2-pentanol y el 3-pentanol son isómeros de posición.
Isómeros de función

semana 21
isomeria
La isomería es una propiedad de aquellos compuestos químicos en especial las cadenas de carbono, que, con igual fórmula molecular (fórmula química no desarrollada) de iguales proporciones relativas de los átomos que conforman su molécula, presentan estructuras químicas distintas, y por ende, diferentes propiedades y configuración. Dichos compuestos reciben la denominación de isómeros. Por ejemplo, el alcohol etílico o etanol y el éter dimetílico son isómeros cuya fórmula molecular es C2H6O.

La isomería es una propiedad de aquellos compuestos químicos en especial las cadenas de carbono, que, con igual fórmula molecular (fórmula química no desarrollada) de iguales proporciones relativas de los átomos que conforman su molécula, presentan estructuras químicas distintas, y por ende, diferentes propiedades y configuración. Dichos compuestos reciben la denominación de isómeros. Por ejemplo, el alcohol etílico o etanol y el éter dimetílico son isómeros cuya fórmula molecular es C2H6O.

miércoles, 23 de mayo de 2018
semana 18
comienzan las expociones de los proyectos
Grupo 1
Mariano perez marrugo
Ricardo rincón echeverry
luis gustavo zuñiga
Brahian camilo arango
Grupo 2
Grupo 1
Ácidos carboxilicos y ésteres
Mariano perez marrugo
Ricardo rincón echeverry
luis gustavo zuñiga
Brahian camilo arango
Grupo 2
Las amidas
juan carlos piedrahita
santiago avendaño
daniel zapata
william perez marrugo
Semana 15
Cadenas carbonadas
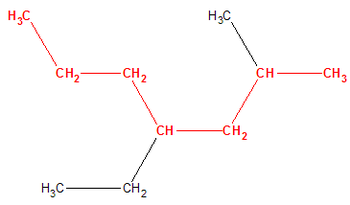
Una cadena carbonada es el esqueleto de prácticamente todos los compuestos orgánicos y está formada por un conjunto de varios átomos de carbono, unidos entre sí mediante enlaces covalentes (carbono-carbono y a la que se unen o agregan otros átomos como hidrógeno, oxígeno o nitrógeno, formando variadas estructuras, lo que origina infinidad de compuestos diferentes.
Semana 14
Actividad de la película ¿ciencia o religión?
Existen los milagros?
En mi opinión si, se han registrado numerosos casos de personas en estado terminal por algún tipo de enfermedad que de la nada mejoran y salen de la zona de riesgo sin ninguna explicación medica
Hay seres de luz?
A día de hoy siguen aumentando los casos de personas que dicen a ver avistado "ángeles" en momentos en los que por ejemplo estuvieron a punto de morir. Aunque no haya una manera de comprobarlo, no creo que esto sea razón para descartar la posibilidad
Se puede dominar la mente?
En mi opinión, el humano usa todos los días el 100% de su cerebro. por lo tanto, se podría decir que la dominamos, sin embargo, la mente es un lugar muy complejo el cual aun no entendemos, por lo que diría que aunque la usemos al 100%, nos faltan bastantes siglos para controlarla
Todos lo científicos son ateos?
No, me parece que es un estereotipo que nos muestra la sociedad, yo en mi cotidianidad he escuchado sobre varios científicos creyentes en dios y milagros .
Semana 13
Se le da a cada equipo su tema a exponer
GRUPO 1
ÁCIDOS CARBOXILICOS
Ricardo rincon
Luis gustavo zuñiga
Brahian camilo arango
Mariana perez marrugo
GRUPO 1
ÁCIDOS CARBOXILICOS
ESTERES
Ricardo rincon
Luis gustavo zuñiga
Brahian camilo arango
Mariana perez marrugo
semana 12
Nomenclatura de los hidrocarburos
Resumiendo, todo el nombre sistemático está estructurado así:
PREFIJO 2º PREFIJO 1º RAIZ SUFIJO 1º SUFIJO 2º
SUFIJO SECUNDARIO
Los grupos funcionales contenidos en la tabla 1. Están ordenados, según lo establecido convencionalmente por laI.U.P.A.C, en orden decreciente de importancia; por ejemplo, si un compuesto en su estructura tiene los grupos
funcionales –COOH, C=O y OH, la función principal es –COOH y las demás son secundarias y por lo tanto, el nombre
del compuesto termina en OICO.
CADENA PRINCIPAL O RAIZ
Es la secuencia carbonada progenitora del compuesto particular y equivale al hidrocarburo no ramificado del mismonúmero de átomos de carbono; dicha secuencia es común para todos los compuestos que resulten de sustituir uno ó más
hidrógenos de ese hidrocarburo por átomos diferentes al carbono y que originan grupos funcionales.
Ejemplo: si el hidrocarburo progenitor es CH 3 CH 2 CH 3 , algunos de sus derivados son: CH 3 CH 2 CH 2 OH
CH 3 CH 2 CH 2 Cl CH 3 CH 2 CH 2 NH 2 (remplazando un H por los grupos funcionales, OH, Cl, NH 2 ) CH 3 CH 2 CHO
(reemplazando 2H por O=)
NUMERACION DE LA SECUENCIA PRINCIPAL
En compuestos con cadena abierta se numera empezando por el extremo más cercano a la función principal, pero enmonociclos se inicia por el vértice donde está la función principal o existe mas ramificación.
Si se presentan dos alternativas de numeración, se comparan término por término las dos secuencias de números y se
selecciona como numeración correcta aquella que presenta el menor número en la primera diferencia.
Si en ambas alternativas se obtienen las mismas secuencias de números, la numeración correcta se da empezando por el
sitio más próximo al primer accidente estructural en orden alfabético.
Es conveniente anotar que los números asignados a enlaces dobles y triples deben ser consecutivos y el menor de ellos
indica su posición.
NOMBRE DE LA RAIZ
El nombre de la raíz se designa mediante un término que indica su número de átomos de carbono, aunque algunas vecesy por eufonía se le adiciona la letra (a) ej. Hept --- Hepta.
PREFIJOS
Son todas las designaciones que aparecen antes de la raízPREFIJO PRIMARIO
Es un término antepuesto a la raíz y relacionado con su naturaleza; se emplean las palabras como ciclo (cadena cerrada)
espirano, biciclo, etc. Pero si la cadena es abierta no se utiliza ningún término.
Semana 11
Grupos funcionales
El grupo funcional es un átomo o conjuntos de átomos unidos a una cadena carbonada, representada en la fórmula general por R para los compuestos alifáticos y como Ar (radicales alifáticos) para los compuestos aromáticos. Los grupos funcionales son responsables de la reactividad y propiedades químicas de los compuestos orgánicos.
La combinación de los nombres de los grupos funcionales con los nombres de los alcanos de los que derivan brinda una nomenclatura sistemática poderosa para denominar a los compuestos orgánicos.
Los grupos funcionales se asocian siempre con enlaces covalentes, al resto de la molécula. Cuando el conjunto de átomos se asocia con el resto de la molécula primero mediante fuerzas iónicas, se denomina como grupo en un conjunto de ion poliatómico o ion complejo.
Radicales
En química, un radical (antes radical libre) es una especie química (orgánica o inorgánica), caracterizada por poseer uno o más electrones desapareados. Se forma en el intermedio de reacciones químicas, a partir de la ruptura homolítica de una molécula y, en general, es extremadamente inestable y, por tanto, con gran poder reactivo y de vida media muy corta (milisegundos).
Semana 9
ciclo del carbono
El ciclo del carbono es un ciclo biogeoquímico por el cual el carbono se intercambia entre la biosfera, la litosfera, la hidrosfera y la atmósfera de la Tierra.Los movimientos anuales de carbono entre reservorios ocurren debido a varios procesos químicos, físicos, geológicos y biológicos.
domingo, 11 de marzo de 2018
semana 8
Alcanos
Los alcanos son hidrocarburos, es decir que tienen sólo átomos de carbono e hidrógeno. La fórmula general para alcanos alifáticos (de cadena lineal) es CnH2n+2, y para cicloalcanos es CnH2n. También reciben el nombre de hidrocarburos saturados de cadena abierta que tiene enlaces sencillos: carbono-carbono y carbono-hidrogeno.
Alquenos
Los alquenos son compuestos insaturados que contienen en su estructura cuando menos un doble enlace carbono-carbono. Fórmula general: CnH2nPor lo tanto, los alquenos sin sustituyen tes tienen el doble de hidrógenos que carbonos. La terminación sistémica de los alquenos es ENO. El más sencillo de los alquenos es el eteno, conocido más ampliamente como etileno, su nombre común. La mayor parte de los alquenos se obtienen del petróleo crudo y mediante la deshidrogenación de los alcanos.
Alquinos
Los alquinos son hidrocarburos insaturados que contienen en su estructura cuando menos un triple enlace carbono-carbono. Fórmula general: CnH2n-2. La terminación sistémica de los alquinos es INO. El más sencillo de los alquinos tiene dos carbonos y su nombre común es acetileno, su nombre sistémico etino.
semana 7
Ciclo de carbono
El ciclo del carbono es el ciclo biogeoquímico por el cual el carbono se intercambia entre la biosfera, pedosfera, geosfera, hidrosfera y la atmósfera de la Tierra. Junto con el ciclo del nitrógeno y el ciclo del agua, el ciclo del carbono comprende una secuencia de eventos que es clave para hacer a la Tierra capaz de sostener vida; describe el movimiento de carbono al ser reciclado y reusado por la biosfera, incluido los sumideros de carbono.

El ciclo del carbono es el ciclo biogeoquímico por el cual el carbono se intercambia entre la biosfera, pedosfera, geosfera, hidrosfera y la atmósfera de la Tierra. Junto con el ciclo del nitrógeno y el ciclo del agua, el ciclo del carbono comprende una secuencia de eventos que es clave para hacer a la Tierra capaz de sostener vida; describe el movimiento de carbono al ser reciclado y reusado por la biosfera, incluido los sumideros de carbono.

semana 6
Química orgánica
La Química orgánica o Química del carbono es la rama de la química que estudia una clase numerosa de moléculas, conocidos como compuestos orgánicos, que contienen carbono formando enlaces covalentes carbono-carbono, carbono-hidrógeno y otros heteroátomos.La teoría vitalista
En el siglo XIX, la química orgánica se definía como la que estudiaba las sustancias de origen vegetal y animal, y los químicos estaban convencidos de que para formar compuestos orgánicos se necesitaba una fuerza vital, creencia conocida como la teoría vitalista.
Surgieron así los postulados del vitalismo, teoría que afirmaba que las sustancias orgánicas solo podían ser generadas por los seres vivos en presencia de la mencionada “fuerza vital”, de orígenes misteriosos, pero nunca a partir de compuestos inorgánicos.
Surgieron así los postulados del vitalismo, teoría que afirmaba que las sustancias orgánicas solo podían ser generadas por los seres vivos en presencia de la mencionada “fuerza vital”, de orígenes misteriosos, pero nunca a partir de compuestos inorgánicos.
Hibridacion
En química, se conoce como hibridación a la interacción de orbitales atómicos dentro de un átomo para formar nuevos orbitales híbridos. Los orbitales atómicos híbridos son los que se superponen en la formación de los enlaces, dentro de la teoría del enlace de valencia, y justifican la geometría molecular.
semana 5
Teoría cinética de los gases
La teoría cinética de los gases explica las características y propiedades de la materia en general, y establece que el calor y el movimiento están relacionados, que las partículas de toda materia están en movimiento hasta cierto punto y que el calor es una señal de este movimiento.La teoría cinética de los gases considera que los gases están compustos por las moléculas, partículas discretas, individuales y separadas. La distancia que existe entre estas partículas es muy grande comparada con su propio tamaño, y el volumen total ocupado por tales corpúsculos es sólo una fracción pequeña del volumen ocupado por todo el gas. por tanto, al considerar el volumen de un gas debe tenerse en cuenta en primer lugar un espacio vacío en ese volumen.El gas deja muchos espacios vacíos y esto explica la alta comprensibilidad, la baja densidad y la gran miscibilidad de unos con otros.
semana 4
Ley de Graham
La ley de Graham, formulada en 1829 por el químico británico Thomas Graham, establece que las velocidades de difusión y efusión de los gases son inversamente proporcionales a las raíces cuadradas de sus respectivas masas molares.
Siendo  las velocidades y
las velocidades y  las masas molares.
las masas molares.
 las velocidades y
las velocidades y  las masas molares.
las masas molares.
Efusión es el flujo de partículas de gas a través de orificios estrechos o poros.
Se hace uso de este principio en el método de efusión de separación de isótopos.
El fenómeno de efusión está relacionado con la energía cinética de las moléculas. Gracias a su movimiento constante, las partículas de una sustancia se distribuyen uniformemente en el espacio libre. Si hay una concentración mayor de partículas en un punto habrá más choques entre sí, por lo que hará que se muevan hacia las regiones de menor número: las sustancias se efunden de una región de mayor concentración a una región de menor concentración
Ley de Gay-Lussac
La ley de Gay-Lussac1 establece que la presión de un volumen fijo de un gas, es directamente proporcional a su temperatura.
- Si el volumen de una cierta cantidad de gas a presión moderada se mantiene constante, el cociente entre presión y temperatura (Centigrados) permanece constante:
o también:
donde:
- P es la presión
- T es la temperatura absoluta (es decir, medida en kelvin)
- k3 una constante de proporcionalidad
domingo, 4 de febrero de 2018
semana 3
Ley de los gases ideales
La ley de los gases ideales es la ecuación de estado del gas ideal, un gas hipotético formado por partículas puntuales sin atracción ni repulsión entre ellas y cuyos choques son perfectamente elásticos (conservación de momento y energía cinética). La energía cinética es directamente proporcional a la temperatura en un gas ideal. Los gases reales que más se aproximan al comportamiento del gas ideal son los gases monoatómicos en condiciones de baja presión y alta temperatura.
La presión ejercida por una fuerza física es inversamente proporcional al volumen de una masa gaseosa, siempre y cuando su temperatura se mantenga constante. o en términos más sencillos:
A temperatura constante, el volumen de una masa fija de gas es inversamente proporcional a la presión que este ejerce. Matemáticamente se puede expresar así:
donde  es constante si la temperatura y la masa del gas permanecen constantes.
es constante si la temperatura y la masa del gas permanecen constantes.
 es constante si la temperatura y la masa del gas permanecen constantes.
es constante si la temperatura y la masa del gas permanecen constantes.
Cuando aumenta la presión, el volumen baja, mientras que si la presión disminuye el volumen aumenta. No es necesario conocer el valor exacto de la constante  para poder hacer uso de la ley: si consideramos las dos situaciones de la figura, manteniendo constante la cantidad de gas y la temperatura, deberá cumplirse la relación:
para poder hacer uso de la ley: si consideramos las dos situaciones de la figura, manteniendo constante la cantidad de gas y la temperatura, deberá cumplirse la relación:
 para poder hacer uso de la ley: si consideramos las dos situaciones de la figura, manteniendo constante la cantidad de gas y la temperatura, deberá cumplirse la relación:
para poder hacer uso de la ley: si consideramos las dos situaciones de la figura, manteniendo constante la cantidad de gas y la temperatura, deberá cumplirse la relación:
Ley de boyle
La ley dice que:
La presión ejercida por una fuerza química es inversamente proporcional a la masa gaseosa, siempre y cuando su temperatura se mantenga constante (si el volumen aumenta la presión disminuye, y si la presión aumenta el volumen disminuye).
o en términos más sencillos:
A temperatura constante, el volumen de una masa fija de gas es inversamente proporcional a la presión que este ejerce.
Matemáticamente se puede expresar así:
donde  es constante si la temperatura y la masa del gas permanecen constantes.1
es constante si la temperatura y la masa del gas permanecen constantes.1
 es constante si la temperatura y la masa del gas permanecen constantes.1
es constante si la temperatura y la masa del gas permanecen constantes.1
Cuando aumenta la presión, el volumen baja, mientras que si la presión disminuye el volumen aumenta. No es necesario conocer el valor exacto de la constante  para poder hacer uso de la ley: si consideramos las dos situaciones de la figura, manteniendo constante la cantidad de gas y la temperatura, deberá cumplirse la relación:
para poder hacer uso de la ley: si consideramos las dos situaciones de la figura, manteniendo constante la cantidad de gas y la temperatura, deberá cumplirse la relación:
 para poder hacer uso de la ley: si consideramos las dos situaciones de la figura, manteniendo constante la cantidad de gas y la temperatura, deberá cumplirse la relación:
para poder hacer uso de la ley: si consideramos las dos situaciones de la figura, manteniendo constante la cantidad de gas y la temperatura, deberá cumplirse la relación:Ley de charles
Volumen sobre temperatura: Constante (K -en referencia a sí mismo)
o también:
donde:
- V es el volumen.
- T es la temperatura absoluta (es decir, medida en Kelvin).
- k2 es la constante de proporcionalidad.
Además puede expresarse como:
semana 2
Propiedades de los gases
En los gases, las fuerzas de atracción son casi inexistentes, por lo que las partículas están muy separadas unas de otras y se mueven rápidamente y en cualquier dirección, trasladándose incluso a largas distancias.
Esto hace que los gases tengan las siguientes propiedades:
1.1- No tienen forma propia
No tienen forma propia, pues se adaptan al recipiente que los contiene.
1.2- Se dilatan y contraen como los sólidos y líquidos.
1.3- Fluidez
Es la propiedad que tiene un gas para ocupar todo el espacio debido a que, prácticamente, no posee fuerzas de unión entre las moléculas que lo conforman
1.4- Difusión
Es el proceso por el cual un gas se mezcla con otro debido únicamente al movimiento de sus moléculas.
Por ejemplo: un escape de gas desde un balón, este tiende a ocupar todo el espacio donde se encuentra mezclándose con el aire.
1.5- Compresión
La compresión es la disminución del volumen de un gas porque sus moléculas se acercan entre sí, debido a la presión aplicada.
Por ejemplo: Se puede observar cuando presionas el émbolo de una jeringa mientras tienes tapada su salida.
1.6- Resistencia
Es la propiedad de los gases de oponerse al movimiento de los cuerpos por el aire. Esto se debe a una fuerza llamada fuerza roce. A mayor tamaño y velocidad del cuerpo mayor es la resistencia.
Por ejemplo: un paracaídas o al elevar un volantín, el roce con el aire impide que el volantín caiga al suelo
jueves, 25 de enero de 2018
Suscribirse a:
Comentarios (Atom)